維生素檢測國標(biāo)法本底污染的原因分析
發(fā)布時(shí)間:
2023-07-17
引言
近年來,檢測行業(yè)中維生素項(xiàng)目的檢驗(yàn)日益增多�。大家在面對維生素復(fù)雜的操作過程時(shí)遇到了各種各樣的問題��,包括樣品稱樣量的計(jì)算��、標(biāo)準(zhǔn)曲線擬合方式的選擇���、樣品稀釋倍數(shù)的選擇�、標(biāo)準(zhǔn)菌的活化等等�����。其中最讓大家頭疼的一個(gè)情況是標(biāo)準(zhǔn)曲線整體渾濁�。造成標(biāo)曲整體渾濁的原因是多種多樣的,但是今年我們又發(fā)現(xiàn)了一個(gè)更隱秘的影響因素���,現(xiàn)分享給大家�,希望大家能避免標(biāo)曲整體渾濁,保證實(shí)驗(yàn)順利進(jìn)行��。
想戰(zhàn)勝你的敵人���,就要了解你的敵人���。維生素的難點(diǎn)到底在哪兒呢?其實(shí)維生素項(xiàng)目的難點(diǎn)很多�,還很細(xì)。追究其核心�����,主要是因?yàn)榫S生素的含量很低����,低到非常容易受到其他因素的干擾。而且這些干擾因素���,看不見���,摸不著�,一個(gè)不留神��,我們就被偷襲了�。結(jié)果就是這樣:
看到此圖時(shí),大部分實(shí)驗(yàn)員估計(jì)已經(jīng)心生絕望�,幾天的辛苦又將付諸東流。所以大部人的反應(yīng)都是趕緊拿遠(yuǎn)點(diǎn)�����,我再也不想多看它一眼����。
但是�����,這是不對的呦����!
我們應(yīng)該積極面對問題,盯著這個(gè)標(biāo)曲�,然后思考。它為啥這么渾濁呢?為啥沒有梯度呢����?為啥標(biāo)曲設(shè)定的時(shí)候要有接種空白和不接種空白呢?好了���,你接近真相了�����!
首先我們要明白標(biāo)曲設(shè)定接種空白和不接種空白的目的����。普通的微生物試驗(yàn)��,我們面臨的只有一個(gè)威脅�����,叫微生物污染�,也叫雜菌污染。但是維生素試驗(yàn)面臨的是兩個(gè)威脅��,一個(gè)是微生物污染��,還有一個(gè)是維生素污染,也叫本底污染����。所以不接種空白用來監(jiān)測的主要是傳統(tǒng)的微生物污染。不接種空白在滅菌后是沒有操作的��,試管不需要打開����,一直保持著滅菌的密閉環(huán)境。如果不接種空白渾濁了���,重點(diǎn)排查滅菌是否徹底�,培養(yǎng)環(huán)境是否污染�。接種空白用來監(jiān)測的主要是維生素污染,以及維生素檢測特有的微生物污染��。所以當(dāng)不接種空白澄清��、接種空白渾濁時(shí)�����,就有兩個(gè)可能性:一是菌不純�����,對維生素沒有單一特定關(guān)系�����,所以不成梯度�。二是試驗(yàn)中混入了除標(biāo)品以外的維生素,促進(jìn)測定菌株生長�,使菌株對樣品中待測維生素或標(biāo)液中維生素失去了特異性,造成標(biāo)曲中各試管標(biāo)品濃度不成梯度����,從而表現(xiàn)為標(biāo)曲試管整體渾濁不成梯度。那么到底是菌的問題還是維生素的問題呢�?●?比如把所有器皿重新洗刷��、酸泡���、高溫烘烤�����;●?比如將標(biāo)準(zhǔn)溶液重新配制���;●?比如驗(yàn)證槍頭�、濾膜等等一次性耗材是否有維生素污染����;但是�����,其實(shí)�����,捷徑就在眼前��。我們?yōu)槭裁床蝗y測那套渾濁的標(biāo)準(zhǔn)試驗(yàn)管呢�?哪怕我們需要壓抑住自己內(nèi)心抗拒的波瀾。
一��、如果我們測出來結(jié)果是這樣的(編撰數(shù)據(jù)):
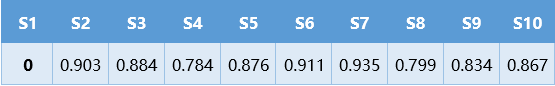
其中S1是不接種空白�����,S2是接種空白�����?����?梢悦黠@的看出:標(biāo)曲各點(diǎn)的吸光度值幾乎一致��,凡是接菌的均明顯生長�����,且沒有任何梯度�。那么結(jié)論也非常明顯,就是測定菌株對待測維生素沒有特異性關(guān)系�����,有兩種可能:一是菌受到了雜菌污染����,在試管內(nèi)生長的以雜菌為主;二是體系中引入不明來源的維生素���。
二����、如果我們測出來結(jié)果是這樣的(編撰數(shù)據(jù)):
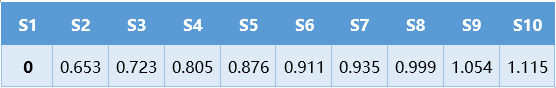
那要恭喜兄臺了!雖然梯度很小���,但是是有的���,只是你的雙眼被蒙蔽了。只有借助紫外分光光度計(jì)才能發(fā)現(xiàn)梯度��。當(dāng)你感激涕零�����,準(zhǔn)備計(jì)算結(jié)果時(shí)�,我只好冷酷的告訴你,這個(gè)標(biāo)曲不能用����。因?yàn)樗捻?xiàng)維生素國標(biāo)里泛酸明確規(guī)定了接種空白吸光度值不能超過0.2,而葉酸2014版曾經(jīng)規(guī)定了接種空白吸光度值不能超過0.1�。GB 5009.210-2016?《食品中泛酸的測定》6.7條款“如果0對照管有明顯的細(xì)菌增長,或者與0對照管相比,標(biāo)準(zhǔn)0管透光率在90%以下(或吸光度值在0.2以上���;或標(biāo)準(zhǔn)系列管透光率最大變化量<40%(或吸光度值變化量<0.4),說明可能有雜菌或不明來源的泛酸混入��,需重做試驗(yàn))”
2022版葉酸�����、維生素B12和2016版生物素��,只對不接種空白有要求��,而對接種空白沒有明確要求����。對沒有明確要求的部分,大家一般會參考同系列標(biāo)準(zhǔn)中對此有要求的標(biāo)準(zhǔn)����,所以嚴(yán)格的話,還是會參考泛酸標(biāo)準(zhǔn)����。畢竟從原理上講,接種空白是不應(yīng)該生長的,現(xiàn)在長到0.653���,畢竟不是最完美狀態(tài)�,對結(jié)果的影響完全未知����。所以最穩(wěn)妥的辦法是找出維生素污染源然后把它清除掉。那么可能的污染源是啥呢��?前文提到了:所有玻璃器皿的潔凈度�;槍頭或移液器的潔凈度;環(huán)境的潔凈度���;標(biāo)品配制的準(zhǔn)確性及稀釋過程的準(zhǔn)確性等等��。不過���,最近小編還發(fā)現(xiàn)了一個(gè)更隱秘的維生素污染源----接種液。
我們維生素試驗(yàn)用到的接種液在接種前都是經(jīng)過特別處理后�����,去除菌液中殘存維生素的�����。比如葉酸通過“饑餓”培養(yǎng)6小時(shí)來清除菌液中殘存葉酸。泛酸��、生物素和維生素B12都是通過“離心-洗脫”三次來去除接種液中殘存維生素�。但是,當(dāng)我們操作不當(dāng)時(shí)會造成接種液中殘存維生素含量遠(yuǎn)遠(yuǎn)超過方法的去除能力����,導(dǎo)致接種液中帶入維生素��,從而污染體系�����,導(dǎo)致維生素本底污染�����,干擾維生素測定�����。
比如:葉酸菌株活化時(shí)我們沒有使用標(biāo)準(zhǔn)要求的4mL葉酸測定培養(yǎng)基加2mL葉酸標(biāo)準(zhǔn)工作液���,而選用了乳酸桿菌肉湯或MRS肉湯進(jìn)行活化�。那結(jié)局是很慘痛的,小編自己也深有體會�。
再比如:生物素和維生素B12菌株活化時(shí)使用的乳酸桿菌肉湯培養(yǎng)基中的番茄汁配制不合規(guī),那也會引起維生素本底的污染��。最近小編就碰到了好幾個(gè)案例�,由于維生素標(biāo)準(zhǔn)中未明確番茄汁的配制方法,所以不少實(shí)驗(yàn)員就用了最直接的思路:番茄整個(gè)榨汁����。這種番茄汁配制后濃度太高,維生素殘留量太大�,超過了離心洗脫能處理的范圍,所以配制后的情況就如下圖所示�。

用直接壓榨的番茄汁配制的培養(yǎng)基活菌,離心后菌體是發(fā)紅的��?��?赡懿煌瑢?shí)驗(yàn)室配制番茄汁濃度會有所不同�����,紅色會有深淺�����,相當(dāng)于番茄的殘留也會有所不同��。但是只要有明顯紅色�����,就說明有不少番茄的殘留被加入了實(shí)驗(yàn)管中�����,那么維生素的殘留就不可避免���,以小編經(jīng)驗(yàn),接種空白吸光度值輕松達(dá)到0.2以上���。而正常合規(guī)的番茄汁配制的培養(yǎng)基活菌離心后��,菌體本身都是白色的��,幾乎見不到紅色��,維生素污染就會控制在要求范圍內(nèi)�。那么合規(guī)的番茄汁應(yīng)該如何配制呢?翻遍食品微生物和維生素相關(guān)標(biāo)準(zhǔn)�����,只有雙歧桿菌檢驗(yàn)的國標(biāo)中有描述:
GB 4789.34-2016?《雙歧桿菌檢驗(yàn)》A.1.2.2條款:“西紅柿浸出液的制備:將新鮮的西紅柿洗凈后稱重切碎���,加等量的蒸餾水在100℃水浴中加熱��,攪拌90min�����,然后用紗布過濾�,校正pH 7.0±0.1����,將浸出液分裝后,121℃高壓滅菌15min-20min�����?��!?/span>
所以各實(shí)驗(yàn)室可以參考此標(biāo)準(zhǔn)配制�����。不過配制過程還是很繁瑣的�����,單一個(gè)煮沸就需要90min�����,所以也可以直接使用陸橋公司的即用型無菌番茄汁(貨號:CMT135���;規(guī)格:100mL/瓶)����。隨用隨加����,無需準(zhǔn)備����,從此遠(yuǎn)離維生素本底污染的困擾,你值得擁有哦�!
看到這里是不是覺得維生素檢測簡直是“步步驚心”��,好好的接種液居然也會暗藏兇險(xiǎn)��。沒辦法���,本質(zhì)上還是因?yàn)闄z測過程中的維生素含量太低了,非常容易受到各種因素的影響�����,所以需要我們提高熟練度��,吸取別人的經(jīng)驗(yàn)教訓(xùn)����,早日攻克維生素實(shí)驗(yàn)的各處難關(guān)。陸橋也提供即用型試管和微孔板法的各項(xiàng)目維生素檢測試劑盒�,幫您少走彎路,避坑繞錯(cuò)�,早日實(shí)現(xiàn)“維生素檢測自由”!